贵州大学刘空军、王培义教授 Angew. Chem. Int. Ed. : 花状超分子聚合物实现生物膜根除、改善叶面亲和力及植物细菌性病害管理
2026-03-16 浏览次数: 10

第一作者:田小雪
通讯作者:刘空军、王培义
通讯单位:1贵州大学 / 绿色农药全国重点实验室;2遵义医科大学
研究速览
由细菌引起的植物病害在防治上长期面临两大难题:生物膜的保护作用使细菌难以被清除,同时传统抗菌剂对叶片表面的亲和力较差,限制了其实际应用效果。近年来,超分子组装体因其能够有效破坏生物膜并具备良好的表面附着能力,逐渐成为一类具有前景的抗菌剂。然而,尽管超分子聚合物在结构和功能调控方面展现出更大的潜力,其在农业病害防控领域的应用仍鲜有报道。本研究构建了一种新型花状超分子聚合物 NOP@CB[8],由新设计的阳离子吡啶盐 NOP 与葫芦[8]脲(CB[8])在水相中自组装形成。NOP@CB[8] 表现出多重协同抗菌机制:能够破坏细菌细胞膜的完整性、干扰细胞内的氧化还原平衡、有效分解已形成的生物膜,并显著增强与植物叶片的亲和性。凭借这些特性,NOP@CB[8] 在盆栽试验中展现出卓越的防治效果。在对水稻细菌性条斑病的防治中,200 µg mL−1 浓度下其保护效果达 56.1%,治疗效果达 51.2%,显著优于 NOP 单体(47.9%/43.1%)和传统药剂噻菌铜(TC,36.2%/33.7%)。值得注意的是,NOP@CB[8] 不仅对目标病原菌表现出优异的抑制活性,其对非靶标生物的安全性也未受到影响;在斑马鱼模型中,其毒性甚至低于游离态的 NOP,显示出良好的环境相容性。进一步将 NOP@CB[8] 应用于柑橘溃疡病和猕猴桃溃疡病的防治,结果表明其保护效果可达约 80%,治疗效果亦超过 60%,效果始终优于 NOP 和 TC。综上所述,本研究为作物病害防控提供了一种绿色高效的替代方案,同时也为发展新型功能超分子聚合物在农业领域的应用开辟了新路径。
要点分析
1.设计与构建
本研究设计了一种含有阳离子吡啶盐和1,3,4-噁二唑的功能分子NOP,通过其与葫芦[8]脲在水中的主客体识别自组装,形成花状超分子聚合物NOP@CB[8]。该结构兼具抗菌和抗生物膜活性,且制备过程绿色环保,无需添加助剂。
2.抗菌机制
NOP@CB[8]通过破坏细菌膜结构、诱导膜电位变化和膜通透性增加,引发细胞内电解质泄漏。同时,它还能抑制抗氧化酶(CAT和SOD)活性,导致活性氧积累,造成氧化损伤,从而增强杀菌效果,优于单一NOP。
3.抗生物膜能力
NOP@CB[8]不仅能抑制生物膜形成,还能有效清除已形成的成熟生物膜。其机制包括抑制胞外多糖合成、降低纤维素酶和淀粉酶活性、削弱细菌运动能力,并通过下调相关基因表达,全面削弱病原菌的致病性。
4.叶面亲和与应用效果
NOP@CB[8]在水稻、柑橘和猕猴桃叶片上表现出优异的润湿、附着和抗冲刷能力。田间试验显示其对水稻白叶枯病、柑橘溃疡病和猕猴桃溃疡病的防效显著优于NOP单体和传统农药噻唑铜,且对作物和非靶标生物安全。
图文导读
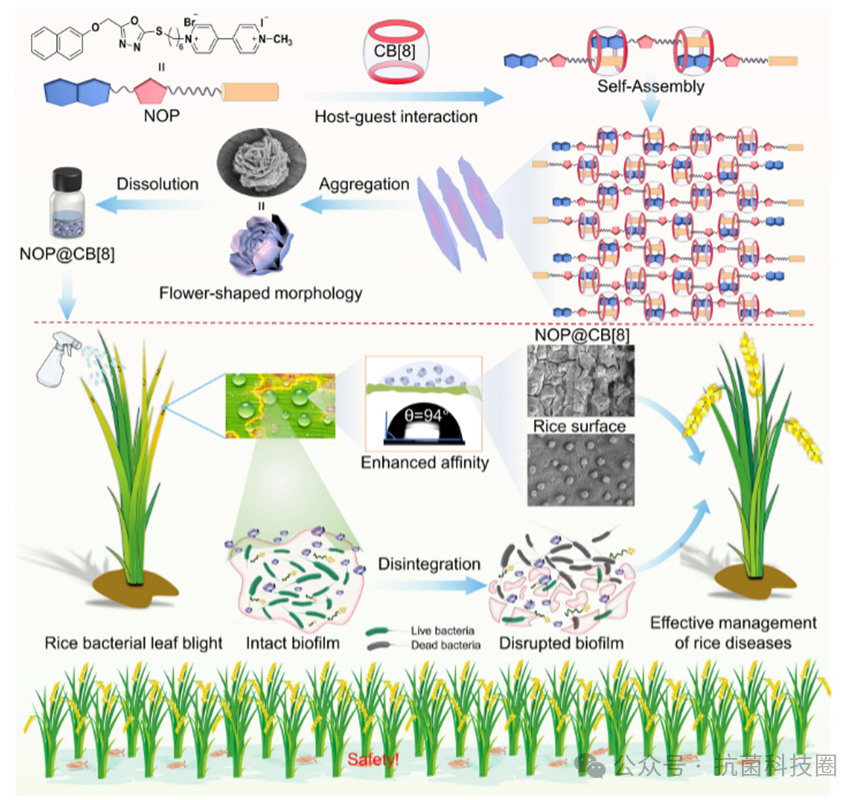
方案 1 :该方案展示了一种类似花朵的超分子聚合物的示意图,它是一种具有生物相容性、多功能的抗菌材料,能够增强叶片上的液滴附着力,消除顽固的生物膜,并有效控制细菌感染。
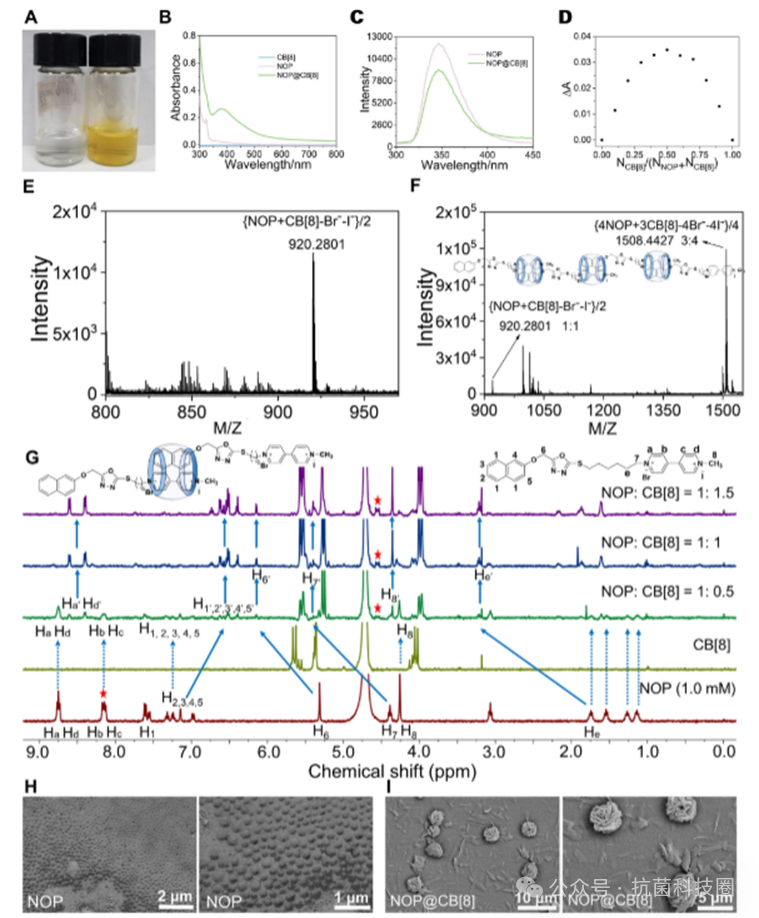
图1 :超分子聚合物 NOP@CB[8] 的表征。(A)NOP(左图)和 NOP@CB[8](右图)在水溶液中的照片。(B)NOP、CB[8] 及其 1:1 混合物(每种 0.15 毫摩尔)在水溶液中的紫外-可见吸收光谱。(C)NOP 和 NOP@CB[8](每种 0.25 毫摩尔)在水溶液中的荧光发射光谱,激发波长为 290 纳米。(D)在水中 NOP 和 CB[8] 总浓度为 0.1 毫摩尔时获得的 350 纳米处的 Job 图。(E、F)NOP@CB[8] 的 MALDI-TOF-MS 光谱。(G)NOP(1.0 毫摩尔)、CB[8] 及其摩尔比为 1:0.5、1:1 和 1:1.5 的混合物的 1H NMR 光谱(400 MHz,D2 O,298 K)。(H、I)NOP(H)和 NOP@CB[8](I)的 SEM 图像。
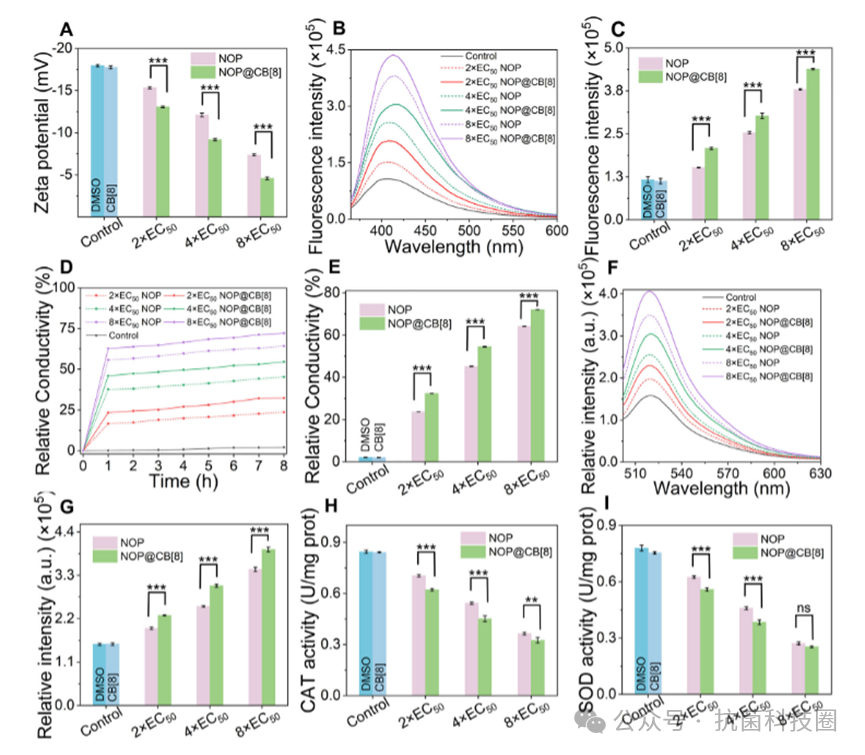
图2:NOP 及其超分子聚合物 NOP@CB[8] 的拟议抗菌机制。(A)不同浓度(0、2×EC50、4×EC50、8×EC50)的 NOP 和 NOP@CB[8] 处理后的 Xoo 细胞的 Zeta 电位。(B)使用 NPN 探针在处理 30 分钟后检测到的 Xoo 外膜通透性的荧光强度曲线(λEx = 350 纳米)。(C)对应于(B)中 NPN 吸收的 415 纳米处的荧光强度定量。(D)不同浓度(0、2×EC50、4×EC50、8×EC50)的 NOP 和 NOP@CB[8] 处理后的 Xoo 悬浮液的相对电导率。(E)从(D)得出的 8 小时后相对电导率的定量值。(F)在不同浓度(0、2×EC50、4×EC50、8×EC50)的 NOP 和 NOP@CB[8] 与 Xoo 共孵育后通过 ROS 试剂盒检测到的 Xoo 内部活性氧(ROS)积累(λEx = 488 纳米)。(G)反映 ROS 水平的 520 纳米处的荧光强度定量。(H、I)在不同浓度的 NOP 和 NOP@CB[8] 处理后 Xoo 中的过氧化氢酶(CAT)和超氧化物歧化酶(SOD)活性。数据以平均值±标准差(n≥3)的形式呈现。统计学意义通过单因素方差分析得出,并随后进行了 LSD 后置检验(*p < 0.05,**p < 0.01,***p < 0.001;ns,无显著差异)。
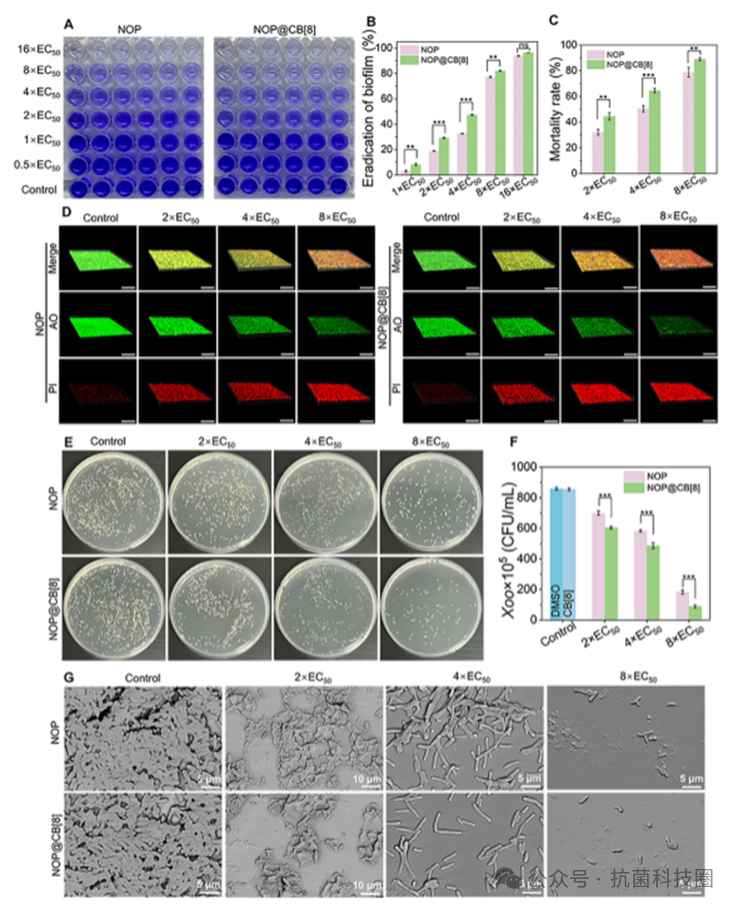
图3:NOP 及其超分子聚合物 NOP@CB[8] 可消除成熟的 Xoo 生物膜。(A、B)使用 NOP 和 NOP@CB[8] 处理后的 Xoo 生物膜的结晶紫染色图像及其定量分析(B)。(C、D)经过各种处理后的 Xoo 生物膜的共聚焦激光扫描显微镜 3D 重建图像(D,比例尺:50 微米)以及相应的荧光强度定量分析(C)。(E、F)Xoo 菌落形成单位的图像(E)以及琼脂平板上菌落数量的统计分析(F)。(G)使用不同浓度的 NOP 和 NOP@CB[8] 进行处理后的 Xoo 生物膜的扫描电子显微镜图像,图像以不同放大倍数显示(所用比例尺:5 或 10 微米)。数据以平均值±标准差的形式呈现(n ≥ 3)。统计学意义通过单因素方差分析得出,并随后进行了 LSD 后置检验(*p < 0.05,**p < 0.01,***p < 0.001;ns,无显著差异)。
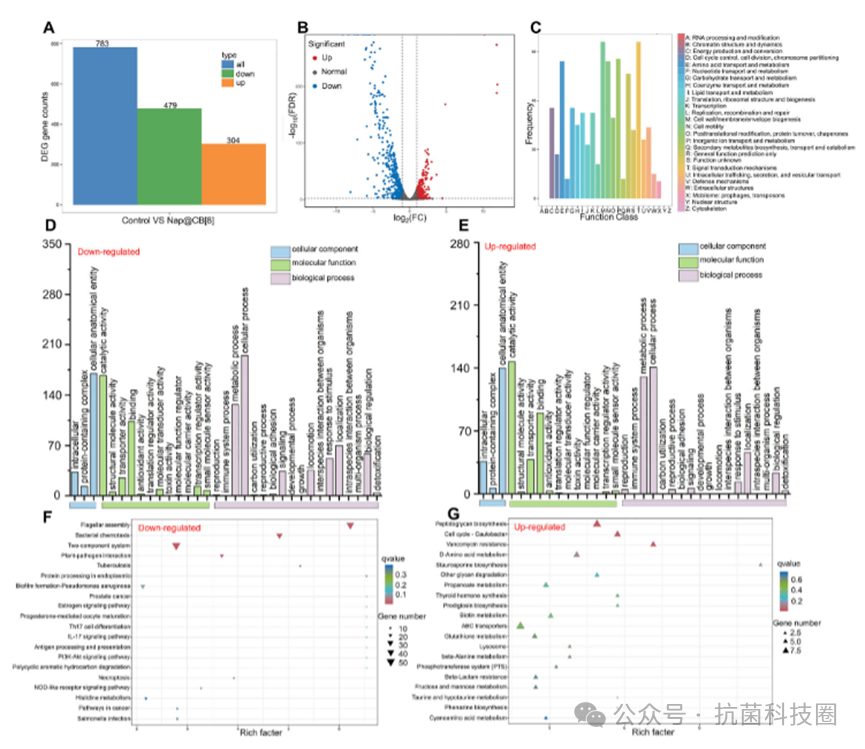
图4:对使用 NOP@CB[8] 在 2 倍 EC50 浓度下处理的 Xoo 组与未处理对照组进行转录组分析。(A)差异表达基因(DEG)统计概览。(B)火山图显示了 DEG 的分布情况。(C)基于(同源基因簇)分类对 DEG 的功能分类。(D、E)下调和上调的 DEG 的 GO 富集分析,以展示功能关联。(F、G)下调和上调的 DEG 的 KEGG 通路富集分析。
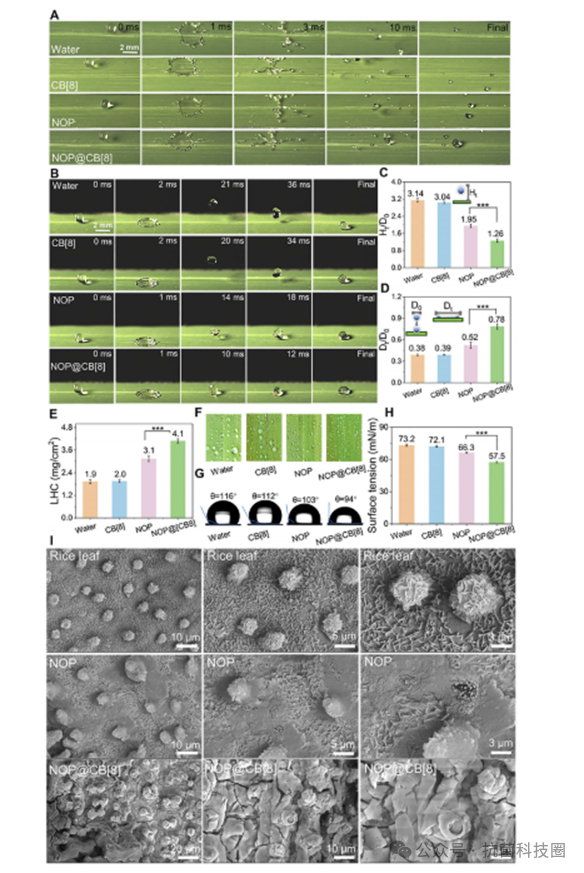
图5:NOP 及其超分子聚合物 NOP@CB[8] 在水稻叶片表面的叶面亲和力。(A、B)从 30 厘米高度滴落形成的液滴高速成像(A)以及从 15 厘米高度反弹的成像(B)。(C)液滴的最大反弹高度,以归一化比率 Ht /D0 表示,源自 Movie S2。(D)液滴相对于其最终铺展状态的归一化铺展直径(Dt /D0),源自 Movie S2。(E)水稻叶片在水、CB[8]、NOP 和 NOP@CB[8] 溶液(200 µg mL− 1)中浸入后的液体持留能力。(F)水、CB[8]、NOP 和 NOP@CB[8] 溶液(200 µg mL− 1)的润湿和铺展行为的可视化观察。(G)水、CB[8]、NOP 和 NOP@CB[8] 溶液(200 µg mL− 1)的接触角。(H)水、CB[8]、NOP 和 NOP@CB[8] 溶液(200 µg mL− 1)的表面张力。(I)显示 NOP 和 NOP@CB[8] 与水稻叶片表面附着情况的扫描电子显微镜图像。NOP 的浓度在自由分子和 NOP@CB[8] 中均为 200 µg mL− 1,后者在 NOP 与 CB[8] 的摩尔比为 1:1 的条件下制备。数据以平均值±标准差(n ≥ 3)的形式呈现。统计学意义通过单因素方差分析得出,并随后进行了 LSD 后置检验(*p < 0.05,**p < 0.01,***p < 0.001;ns,无显著差异)。
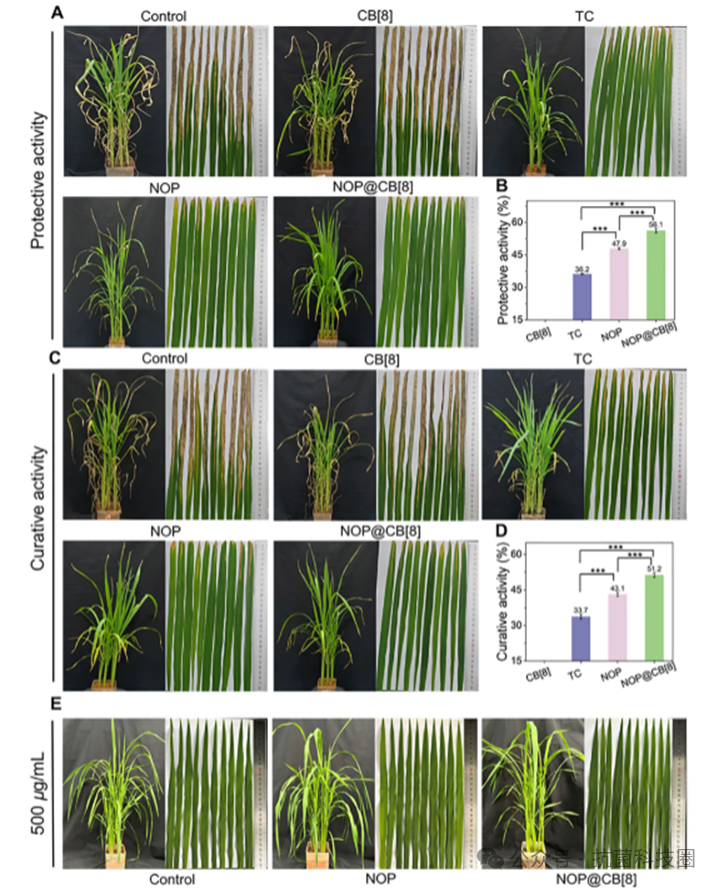
图6:NOP 及其超分子聚合物 NOP@CB[8] 在水稻细菌叶枯病防治中的体内疗效及安全性研究。(A、C)在连续培养 14 天后,使用 NOP、NOP@CB[8] 或商业杀菌剂 TC(200 µg ⋅mL− 1 )处理水稻叶片后的病害症状代表性图像。(B)基于(A)中所示的病斑严重程度对每种处理的保护效果进行定量评估。(C)从(B)中得出的 NOP、NOP@CB[8] 和 TC 的治愈效果定量评估。(D)在 500 µg mL− 1 浓度下,NOP 和 NOP@CB[8] 对水稻植株的药害评估。NOP 的浓度在自由分子和 NOP@CB[8] 中均为 200 µg mL− 1 ,后者中 NOP 与 CB[8] 的摩尔比为 1:1。数据以平均值±标准差(n ≥ 3)的形式呈现。统计学意义通过单因素方差分析得出,并随后进行了 LSD 后置检验(*p < 0.05,**p < 0.01,***p < 0.001;ns,无显著差异)。
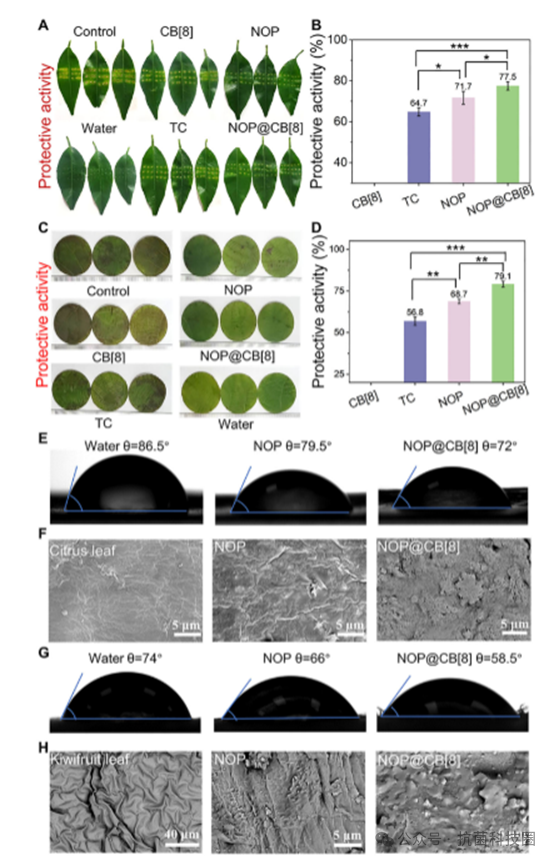
图 7: NOP 及其超分子聚合物 NOP@CB[8] 对柑橘和猕猴桃溃疡病的体内疗效,以及它们在相应叶片上的叶面亲和性。(A)应用 NOP、NOP@CB[8] 和商业杀菌剂 TC(200 µg ⋅mL− 1 )处理柑橘叶片 14 天后,连续培养期间病害症状的代表性图像。(B)基于(A)中所示的病变严重程度对每种处理的保护效果进行定量。(C)应用 NOP、NOP@CB[8] 和 TC(200 µg ⋅mL− 1 )处理猕猴桃叶片 14 天后,连续培养期间病害症状的代表性图像。(D)从(C)中得出的每种处理的保护效果定量结果。(E) NOP 和 NOP@CB[8] 溶液在柑橘叶片上的接触角。(F)显示 NOP 和 NOP@CB[8] 与柑橘叶片表面附着情况的扫描电子显微镜图像。(G) NOP 和 NOP@CB[8] 溶液在猕猴桃叶片上的接触角。(H)显示 NOP 和 NOP@CB[8] 与猕猴桃叶片表面附着情况的扫描电子显微镜图像。NOP 的浓度在自由分子和 NOP@CB[8] 中均为 200 µg mL− 1 ,后者以 NOP 与 CB[8] 的 1:1 摩尔比制备。数据以均值±标准差的形式呈现(样本数量≥3)。统计学意义通过单因素方差分析得出,并随后进行了 LSD 后置检验(*p < 0.05,**p < 0.01,***p < 0.001;ns,无显著差异)。
结论
本研究首次报道了一种基于主客体识别自组装的超分子聚合物NOP@CB[8],并将其成功应用于植物细菌性病害的防控。该聚合物由作者自主设计的功能分子NOP与葫芦[8]脲在水相中自组装而成,形成具有花状形貌的超分子结构。NOP@CB[8]不仅保留了NOP本征的抗菌活性,还通过CB[8]的引入显著增强了其对细菌细胞膜的破坏能力和抗氧化系统的干扰作用,表现出优于单体的杀菌效果。更重要的是,该聚合物在生物膜形成的多个关键环节——包括胞外多糖合成、胞外酶活性、细菌运动能力等方面均表现出显著的抑制作用,具备抑制和清除成熟生物膜的双重功能。
此外,NOP@CB[8]在水稻、柑橘和猕猴桃叶片表面展现出优异的润湿性、附着性和抗雨水冲刷能力,显著提升了药剂的叶面利用率。田间试验结果表明,其对水稻白叶枯病、柑橘溃疡病和猕猴桃溃疡病的防效均优于NOP单体和传统药剂噻唑铜,且对作物本身和非靶标生物如斑马鱼表现出良好的安全性。该研究不仅为植物病害防控提供了一种高效、环保的新型超分子材料,也为未来开发多功能、智能响应的绿色农药平台奠定了理论基础和实验依据。
(来源:抗菌科技圈)